Вектибикс конц д/р-ра д/инф 20мг/мл 5мл №1
- Артикул:
- 10036291
- Действующие вещества:
- Панитумумаб
- Производитель:
- Amgen Europe B.V.
- Представительство:
- Евросервис
- Форма выпуска:
- концентрат для приготовления раствора для инфузий
- Потребительская категория:
- Моноклональные антитела
- В упаковке:
- 1 шт. / 27825 ₽ за 1 шт.
-
Доставка в 137 аптек в Москве и Московской области
Получение 28 мая - БесплатноАптеки -
Оплата при получении наличными или картой
-
Срок хранения заказа 5 дней
-
Доставка в 137 аптек в Москве и Московской области
Получение 28 мая - БесплатноАптеки -
Оплата при получении наличными или картой
-
Срок хранения заказа 5 дней

1 мл концентрата содержит:
активное вещество: панитумумаб - 20 мг
вспомогательные вещества: натрия ацетата тригидрат - 6,8 мг, натрия хлорид - 5,8 мг, уксусная кислота ледяная - до pH 5,8, вода для инъекций - достаточное количество.При применении препарата Вектибикс в качестве монотерапии или в комбинации с химиотерапией фармакокинетика препарата носит нелинейный характер.
После однократного введения панитумумаба в виде 1-часовой инфузии площадь под кривой «концентрация-время» (AUC) возрастала в большей степени, чем это характерно при дозопропорциональной зависимости, а клиренс (CL) панитумумаба снижался с 30,6 до 4,6 мл/сут/кг при увеличении дозы от 0,75 до 9 мг/кг. Однако при введении панитумумаба в дозах свыше 2 мг/кг характер увеличения AUC был близок к дозопропорциональной зависимости.
При соблюдении рекомендованного режима дозирования (6 мг/кг 1 раз в 2 недели в виде 1-часовой инфузии) равновесная концентрация панитумумаба достигается к третьей инфузии при средних значениях максимальной (± стандартное отклонение [SD]) и минимальной концентраций 213 ± 59 и 39 ± 14 мкг/мл, соответственно. Среднее значение (± SD) AUC0-τ И клиренса были равны 1306 ± 374 мкг*сут/мл и 4,9 ± 1,4 мл/кг/сут, соответственно.
Период полувыведения препарата составил приблизительно 7,5 суток (разброс: от 3,6 до 10,9 суток).
Был выполнен популяционный анализ фармакокинетики с целью оценки потенциального влияния отдельных ковариат на параметры фармакокинетики панитумумаба. Результаты его показали, что возраст (в диапазоне 21-88 лет), пол, раса, функция печени и почек, применение сопутствующих химиотерапевтических препаратов и интенсивность окрашивания мембран EGFR (1+, 2+, 3+) в опухолевых клетках не оказывают явного влияния на фармакокинетику панитумумаба.
Исследований фармакокинетики панитумумаба у пациентов с нарушением функций почек или печени не проводилось.
- в качестве первой линии терапии в комбинации с режимами, содержащими фторурацил, кальция фолинат и оксалиплатин (FOLFOX) или фторурацил, кальция фолинат и иринотекан (FOLFIRI);
- в качестве второй линии терапии в комбинации с режимом, содержащим фторурацил, кальция фолинат и иринотекан (FOLFIRI) у пациентов, получавших ранее химиотерапию первой линии на основе фторпиримидина (исключая иринотекан);
- в качестве монотерапии при неэффективности режимов химиотерапии на основе фторпиримидина, оксалиплатина и иринотекана.
- Пациенты с анамнезом тяжелых или угрожающих жизни реакций гиперчувствительности к действующему веществу или любому из вспомогательных веществ препарата, перечисленных в разделе «Состав» (см. раздел «Особые указания»);
- Пациенты с интерстициальным пневмонитом или фиброзом легких (см. раздел «Особые указания»);
- Комбинация препарата Вектибикс с оксалиплатин-содержащим режимом химиотерапии противопоказана пациентам с мКРР и мутациями в генах RAS или пациентам с мКРР с неуточненным статусом мутаций в генах RAS (см. раздел «Особые указания»);
- Пациенты с почечной и печеночной недостаточностью (эффективность и безопасность применения не установлены);
- Детский возраст до 18 лет (эффективность и безопасность применения не установлены; см. раздел «Способ применения и дозы»);
- Беременность и период грудного вскармливания (эффективность и безопасность применения не установлены; см. раздел «Применение при беременности и в период грудного вскармливания»).
- У пациентов с кератитом, язвенным кератитом или выраженной сухостью глаз (см. раздел «Особые указания»).
Терапию препаратом Вектибикс необходимо проводить под контролем врача, имеющего опыт проведения противоопухолевого лечения. Перед началом терапии препаратом Вектибикс необходимо подтверждение гена RAS дикого типа (KRAS и NRAS). Мутационный статус гена должен быть определен лабораторией, имеющей опыт соответствующих исследований, с использованием валидированных методик обнаружения мутаций KRAS (в экзонах 2, 3 и 4) и NRAS (в экзонах 2, 3 и 4).
Режим дозирования
Рекомендуемая доза препарата Вектибикс составляет 6 мг/кг массы тела и вводится 1 раз в 2 недели.
При развитии тяжелых (≥ 3 степени) дерматологических реакций может потребоваться следующий режим модификации дозы препарата Вектибикс:
|
Возникновение кожных симптомов: ≥степени 31 |
Введение препарата Вектибикс |
Результат |
Коррекция дозы |
|
Первый случай возникновения |
Отмена 1 или 2 доз |
Снижение интенсивности реакции (<3 степени) |
Возобновление инфузии в дозе, составляющей 100% от первоначальной дозы |
|
Улучшения не наступило |
Прекращение |
||
|
Второй случай возникновения |
Отмена 1 или 2 доз |
Снижение интенсивности реакции (<3 степени) |
Возобновление инфузии в дозе, составляющей 80% от первоначальной дозы |
|
Улучшения не наступило |
Прекращение |
||
|
Третий случай возникновения |
Отмена 1 или 2 доз |
Снижение интенсивности реакции (<3 степени) |
Возобновление инфузии в дозе, составляющей 60% от первоначальной дозы |
|
Улучшения не наступило |
Прекращение |
||
|
Четвертый случай возникновения |
Прекращение |
- |
- |
1 Реакции 3 степени и выше считаются тяжелыми или жизнеугрожающими.
Применение у отдельных популяций пациентов
Безопасность и эффективность препарата Вектибикс не оценивались у пациентов с почечной или печеночной недостаточностью. Отсутствуют клинические данные, позволяющие обосновать необходимость коррекции дозы препарата в пожилом возрасте.
Дети
Опыт применения препарата Вектибикс у детей отсутствует.
Способ введения
Вектибикс необходимо вводить в виде внутривенной инфузии с помощью инфузионного насоса.
Перед проведением инфузии препарат Вектибикс должен быть разведен специалистом здравоохранения в 9 мг/мл (0,9%) растворе натрия хлорида для инъекций в асептических условиях до получения конечной концентрации не более 10 мг/мл. Не встряхивать или не взбалтывать сильно флакон. Флакон с препаратом Вектибикс следует визуально оценить перед применением. Раствор должен быть бесцветным и может содержать полупрозрачные или белые аморфные белковые частицы (которые удаляются фильтром инфузионной системы). Не следует вводить препарат Вектибикс, описание которого отличается от приведенного выше. При помощи гиподермальной иглы размера 21G или меньше из флакона с препаратом забирается необходимое количество препарата Вектибикс для получения дозы 6 мг/кг, которое затем растворяют в общем объеме 100 мл. Не использовать безыгольные приспособления (например, переходники для флаконов) для извлечения препарата из флакона. Конечная концентрация не должна превышать 10 мг/мл. Дозы выше, чем 1000 мг следует растворить в 150 мл 9 мг/мл (0,9%) раствора натрия хлорида для инъекций. Полученный разведенный раствор необходимо перемешать осторожным переворачиванием, не встряхивать.
Не наблюдалось несовместимости между препаратом Вектибикс и 9 мг/мл (0,9%) раствором натрия хлорида для инъекций в инфузионных пакетах из поливинилхлорида или полиолефина.
Препарат Вектибикс следует вводить в периферический зонд или постоянный катетер через встроенный фильтр с размером пор 0,2 или 0,22 мкм с низкой степенью связывания белков. Рекомендованная длительность инфузии составляет приблизительно 60 минут. Если первая инфузия переносится хорошо, последующие инфузии могут производиться в течение 30-60 минут. Длительность введения препарата в дозах свыше 1000 мг должна составлять приблизительно 90 минут (инструкции по обращению приведены в подразделе «Особые меры предосторожности при применении и утилизации»).
До и после введения препарата Вектибикс, инфузионную систему необходимо промыть раствором натрия хлорида, чтобы избежать смешивания препарата Вектибикс с другими лекарственными препаратами или растворами для внутривенного введения.
В случае возникновения инфузионных реакций может потребоваться снижение скорости инфузии препарата Вектибикс (см. раздел «Особые указания»).
Препарат Вектибикс не должен вводиться струйно или болюсно.
Хранить при температуре от 2°С до 8°С. Не замораживать. Хранить в оригинальной упаковке для защиты от света. Хранить в недоступном для детей месте!
3 года. Не использовать по истечении срока годности, указанного на упаковке.
Отслеживаемость
С целью улучшения отслеживаемости биологических лекарственных препаратов следует точно записывать название и номер серии вводимого препарата.
Нежелательные реакции со стороны мягких тканей и кожи
Дерматологические реакции - фармакологический эффект, характерный для ингибиторов EGFR, регистрируются практически у всех пациентов (приблизительно 94%), получающих препарат Вектибикс. Тяжелые кожные реакции (3 степени согласно классификации NCI-CTC) отмечались у 23% пациентов, жизнеугрожающие кожные реакции (4 степени NCI-CTC) - у < 1% пациентов, принимавших препарат Вектибикс в качестве монотерапии и в комбинации с химиотерапией (n = 2224) (см. раздел «Побочное действие»). При развитии у пациента кожных реакций степени 3 (Общие терминологические критерии оценки нежелательных явлений СТСАЕ, версия 4.0) или более выраженной степени, либо расцененных как непереносимые, см. рекомендации по модификации дозы в разделе «Способ применения и дозы».
В клинических исследованиях после развития тяжелых кожных реакций (в том числе стоматита) имели место инфекционные осложнения, в том числе сепсис и некротизирующий фасциит, которые в редких случаях приводили к смерти, а также к образованию абсцессов, требовавших вскрытия и дренирования.
Пациенты, у которых отмечались тяжелые кожные реакции или проявления токсичности со стороны мягких тканей, либо демонстрировавшие усугубление данных реакций на фоне терапии препаратом Вектибикс, должны наблюдаться на предмет развития воспалительных или инфекционных последствий (в том числе воспаление подкожной клетчатки и некротизирующего фасциита), а при наличии соответствующих клинических показаний должна быть начата соответствующая терапия. Жизнеугрожающими и летальными инфекционными осложнениями являлись некротизирующий фасциит и сепсис, которые отмечались у пациентов, получавших препарат Вектибикс. Редкие случаи синдрома Стивенса-Джонсона и токсического эпидермального некролиза отмечались у пациентов в пострегистрационном периоде, принимавших препарат Вектибикс. Временная отмена или прекращение применения препарата Вектибикс необходимы при развитии кожной токсичности или токсичности мягких тканей, ассоциированных с развитием тяжелых или жизнеугрожающих воспалительных или инфекционных осложнений.
Лечение и ведение дерматологических реакций должно быть основано на тяжести проявлений и может включать в себя увлажняющие, солнцезащитные средства (солнцезащитный фильтр > 15 UVA и UVB), а также кремы с глюкокортикостероидами (не выше 1% гидрокортизона) для применения на пораженных участках и/или пероральные антибиотики (например, доксициклин). Также пациентам с признаками сыпи/дерматологической токсичности рекомендуется использовать солнцезащитные средства и головные уборы, ограничить пребывание на солнце, поскольку солнечный свет может усилить любые возможные кожные реакции.
Пациентам может быть рекомендовано наносить увлажняющие, солнцезащитные средства на лицо, руки, ноги, шею, спину и грудь каждое утро, а на ночь наносить крем, содержащий глюкокортикостероид, на лицо, руки, ноги, шею, спину и грудь во время проведения лечения.
Осложнения со стороны легких
Пациенты с наличием в анамнезе или имеющие признаки интерстициального пневмонита или фиброза легких исключались из клинических исследований. Случаи интерстициальных заболеваний легких с летальными исходами и без, возникали, преимущественно, в японской популяции. Поэтому при остром возникновении или ухудшении легочных симптомов лечение препаратом Вектибикс должно быть приостановлено и незамедлительно начато изучение возникших симптомов. При обнаружении интерстициальных заболеваний легких препарат Вектибикс следует временно отменить и назначить соответствующее лечение. У пациентов с интерстициальным пневмонитом или легочным фиброзом в анамнезе необходимо оценить отношение вероятной пользы применения препарата к риску осложнений со стороны легких.
Нарушения водно-электролитного баланса
У некоторых пациентов отмечалось прогрессивное снижение сывороточных концентраций магния, приводившее к тяжелой (степень 4) гипомагниемии. Необходим периодический мониторинг состояния пациентов на предмет развития гипомагниемии и сопутствующей гипокальциемии перед началом лечения препаратом Вектибикс, и после лечения до 8 недель после его окончания (см. раздел «Побочное действие»). При необходимости рекомендован
прием препаратов магния.
Также отмечались нарушения баланса других электролитов, включая гипокалиемию. Рекомендуется мониторинг и соответствующий адекватный прием данных электролитов.
Инфузионные реакции
В клинических исследованиях монотерапии и комбинированной терапии мКРР (n = 2224), инфузионные реакции, в том числе тяжелые инфузионные реакции (возникавшие в течение 24 часов после инфузии), отмечались у пациентов, получавших препарат Вектибикс (степень 3 и 4 по NCI-CTC).
В пострегистрационных исследованиях сообщалось о серьезных инфузионных реакциях, включая редкие пострегистрационные сообщения о летальных исходах. В случае возникновения тяжелой или жизнеугрожающей реакции в процессе инфузии или в любое время после ее завершения [например, при возникновении бронхоспазма, ангионевротического отека, гипотензии, потребности в парентеральной терапии или анафилаксии], необходимо полностью отменить препарат Вектибикс (см. разделы «Противопоказания» и «Побочное действие»).
У пациентов с легкими или умеренными (степень 1 и 2 по СТСАЕ версии 4.0) инфузионными реакциями следует уменьшить скорость инфузии на протяжении всей инфузии. Рекомендуется сохранять сниженную скорость инфузии в ходе всех последующих инфузий.
Сообщалось о реакциях гиперчувствительности, возникавших более чем через 24 часа после инфузии, включая ангионевротический отек со смертельным исходом, развившийся более чем через 24 часа после инфузии. Следует предупредить пациентов о возможности позднего развития реакции и проинструктировать обращаться к своему лечащему врачу в случае возникновения симптомов реакции гиперчувствительности.
Острая почечная недостаточность
Острая почечная недостаточность отмечена у пациентов с тяжелой диареей и дегидратацией. Пациенты должны быть проинструктированы о необходимости немедленно обратиться за медицинской помощью при развитии тяжелой диареи.
Препарат Вектибикс в комбинации с химиотерапией на основе иринотекана, фторурацила болюсно и кальция фолината (режим IFL)
У пациентов, получавших препарат Вектибикс в комбинации с режимом IFL [болюсное введение фторурацила (500 мг/м2), кальция фолината (20 мг/м2) и иринотекана (125 мг/м2)], отмечалась высокая частота тяжелой диареи (см. раздел «Побочное действие»). Поэтому следует избегать использования препарата Вектибикс в комбинации с режимом IFL (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Препарат Вектибикс в комбинации с бевацизумабом и режимами химиотерапии
У пациентов, получавших препарат Вектибикс в комбинации с бевацизумабом и химиотерапией, отмечалось укорочение выживаемости без прогрессирования заболевания и повышение частоты летальных исходов. Кроме того, в группах терапии препаратом Вектибикс в комбинации с бевацизумабом и химиотерапией отмечалось повышение частоты тромбоэмболии легочной артерии, инфекций (преимущественно кожных), диареи, электролитных нарушений, тошноты, рвоты и дегидратации. Препарат Вектибикс не должен применяться в комбинации с химиотерапией, включающей бевацизумаб (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Препарат Вектибикс в комбинации с химиотерапией на основе оксалиплатина у пациентов с мКРР и мутациями RAS, а также с неуточненным статусом RAS
Комбинация препарата Вектибикс с химиотерапией на основе оксалиплатина противопоказана пациентам с мКРР и мутациями RAS, а также пациентам с мКРР с неуточненным статусом мутаций генов RAS (см. раздел «Противопоказания»).
Отмечалось сокращение выживаемости без прогрессирования заболевания (ВБП) и общей выживаемости (ОВ) у пациентов с мутациями KRAS (в экзоне 2) в опухоли и дополнительными мутациями RAS (KRAS [в экзонах 3 и 4] или NRAS [в экзонах 2, 3, 4]), получавших панитумумаб в комбинации с инфузионным режимом, содержащим фторурацил, кальция фолинат и оксалиплатин (FOLFOX) по сравнению с пациентами, получавшими только FOLFOX.
Оценка мутационного статуса RAS должна определяться с использованием валидированного метода в лаборатории, имеющей опыт выполнения подобных исследований (см. раздел «Способ применения и дозы»). Если препарат Вектибикс должен использоваться в комбинации с режимом FOLFOX, рекомендуется определение мутационного статуса в лаборатории, принимающей участие в программе внешнего обеспечения качества оценки статуса
RAS, либо дикий тип должен быть подтвержден результатами двукратного анализа.
Офтальмологическая токсичность
Отмечались серьезные случаи кератита и язвенного кератита, которые могут приводить к перфорации роговицы. Пациенты, у которых отмечаются признаки и симптомы, свидетельствующие о наличии кератита, в том числе острые или усугубляющиеся: воспалительные изменения глаза, слезотечение, светобоязнь, снижение четкости зрения, боли в глазу и/или покраснения глаза, должны быть немедленно направлены к офтальмологу.
При подтверждении диагноза язвенного кератита терапию препаратом Вектибикс необходимо временно или полностью прекратить. При постановке диагноза кератита необходимо тщательно соотнести пользу и риски продолжения терапии. Препарат Вектибикс должен использоваться с осторожностью у пациентов, имевших в анамнезе кератит, язвенный кератит или выраженную сухость глаза. Использование контактных линз также
является фактором риска развития кератита и изъязвлений.
Пациенты с показателем общего состояния 2 по шкале ECOG, получавших препарат Вектибикс в комбинации с химиотерапией
Для пациентов с мКРР, имеющих показатель 2 по шкале ECOG, рекомендуется проведение оценки соотношения польза-риск до начала применения препарата Вектибикс в комбинации с химиотерапией. У пациентов со статусом ECOG 2 не выявлено положительное соотношение польза-риск.
Пожилые пациенты
Различий безопасности или эффективности препарата Вектибикс в монотерапии у пациентов пожилого возраста (≥ 65 лет) не наблюдалось. Однако отмечалось увеличение количества серьезных нежелательных реакций у пожилых пациентов, получавших препарат Вектибикс в комбинации с химиотерапией FOLFIRI или FOLFOX, по сравнению с применением только режимов химиотерапии (см. раздел «Побочное действие»).
Предупреждение о вспомогательных веществах
Данный препарат содержит 3,45 мг натрия в 1 мл, что соответствует 0,017% от рекомендованного ВОЗ максимального суточного потребления натрия для взрослого человека, составляющего 2 г.
Особые меры предосторожности при применении и утилизацииПрепарат Вектибикс следует вводить в периферический зонд или постоянный катетер через встроенный фильтр с размером пор 0,2 или 0,22 мкм с низкой степенью связывания белков.
Разведенный раствор
Вектибикс не содержит антимикробных консервантов или бактериостатических агентов. Препарат должен быть использован непосредственно после разведения. Если препарат не был использован сразу после разведения, пользователь несет ответственность за время и условия его хранения до следующего введения (не более 24 часов при температуре 2°С - 8°С). Не замораживать разведенный раствор.
Препарат Вектибикс предназначен только для однократного использования.
Флакон и оставшийся в нем раствор лекарственного препарата необходимо утилизировать после однократного применения.
Весь неиспользованный остаток препарата и расходные материалы должны утилизироваться в соответствии с надлежащими требованиями.
Противоопухолевое средство, моноклональные антитела.
Исследования in vitro и in vivo на животных показали, что панитумумаб ингибирует рост и выживаемость опухолевых клеток, экспрессировавших EGFR. Не наблюдалось противоопухолевой активности панитумумаба в экспериментах с ксенотрансплантатами опухолей человека, не экспрессировавшими EGFR. Добавление панитумумаба к лучевой, химио- или другой таргетной терапии в исследованиях на животных приводило к усилению противоопухолевого эффекта по сравнению с только лучевой, химио- или таргетной терапией.
Кожные реакции (в том числе проявления на ногтях) отмечались у пациентов, получавших препарат Вектибикс или другие ингибиторы EGFR, и, как известно, ассоциированы с фармакологическими эффектами терапии (см. разделы «Способ применения и дозы» и «Побочное действие»).
Иммуногенность
Как и все терапевтические протеины, панитумумаб обладает потенциальной иммуногенностью. Продукцию анти-панитумумаб антител оценивали с помощью двух различных скрининговых систем иммуноанализа для определения связывающих анти-панитумумаб антител (ИФА - иммуноферментный анализ, который позволяет определить высокоаффинные антитела, и биосенсорный иммуноанализ, позволяющий определить высоко- и низкоаффинные антитела). Пациентам, чья сыворотка оказывалась положительной в любом из двух тестов скринингового иммуноанализа, проводился также биологический тест in vitro для обнаружения нейтрализующих антител.
В качестве монотерапии:
- Выявляемость связывающих антител (за исключением случаев выявления антител до введения препарата и временно положительных) составляла <1%, как было установлено с помощью анализа ИФА методом кислотной диссоциации, и 3,8%, как было установлено с помощью иммунологического анализа Biacore;
- Выявляемость нейтрализующих антител (за исключением случаев выявления антител до введения препарата и временно положительных) составляла <1%;
- При сравнении с пациентами, у которых антитела не вырабатывались, взаимосвязь между наличием анти-панитумумаб антител и изменениями фармакокинетических параметров, эффективности и безопасности препарата отмечена.
В комбинации с режимами химиотерапии на основе иринотекана или оксалиплатина:
- Выявляемость связывающих антител (за исключением случаев выявления антител до введения препарата) составляла 1%, как было установлено с помощью анализа ИФА методом кислотной диссоциации, и < 1%, как было установлено с помощью иммунологического анализа Biacore;
- Выявляемость нейтрализующих антител (за исключением случаев выявления антител до введения препарата) составляла <1%;
- Не было обнаружено никаких доказательств изменения профиля безопасности у пациентов с положительным результатом теста на антитела к препарату Вектибикс.
Определение образования антител зависит от чувствительности и специфичности используемого метода. На положительный результат по определению антител могут оказать влияние различные факторы, включая метод проведения анализа, методику отбора и подготовку образцов, время забора проб, прием сопутствующих лекарственных препаратов и характер основного заболевания, поэтому сравнение частоты возникновения антител к другим препаратам может приводить к недостоверным результатам.
Согласно результатам анализа данных всех пациентов с мКРР, принимавших участие в клинических исследованиях и получавших препарат Вектибикс в режиме монотерапии и в комбинации с химиотерапией (n = 2224) наиболее частыми нежелательными реакциями были кожные реакции, наблюдавшиеся приблизительно в 94% случаев. Эти реакции обусловлены фармакологическими свойствами препарата Вектибикс и обычно имеют легкую или среднюю степень тяжести; только в 23% случаев дерматологические реакции носят тяжелый характер (степень тяжести 3, по классификации NCI-CTC) и < 1% жизнеугрожающие (степень 4 по NCI-CTC). Медицинские меры в случае кожных реакций, включая рекомендации по коррекции дозы, приведены в разделе «Особые указания».
Наиболее частыми нежелательными реакциями, возникавшими у ≥ 20% пациентов, были расстройства желудочно-кишечного тракта [диарея (46%), тошнота (39%), рвота (26%), запор (23%) и боль в животе (23%)]; общие реакции [повышенная утомляемость (35%), пирексия (21%)]; нарушения обмена веществ и питания [снижение аппетита (30%)]; инфекции и инвазии [паронихия (20%)]; и патология кожи и подкожной ткани [сыпь (47%), акнеформный дерматит (39%), зуд (36%), эритема (33%) и сухость кожи (21%)].
Перечень нежелательных реакций
Нежелательные реакции, наблюдавшиеся у пациентов с мКРР, получавших панитумумаб в качестве монотерапии или в комбинации с химиотерапией в клинических исследованиях (n = 2224), а также в спонтанных сообщениях, приведены ниже. Нежелательные эффекты представлены по степени убывания серьезности.
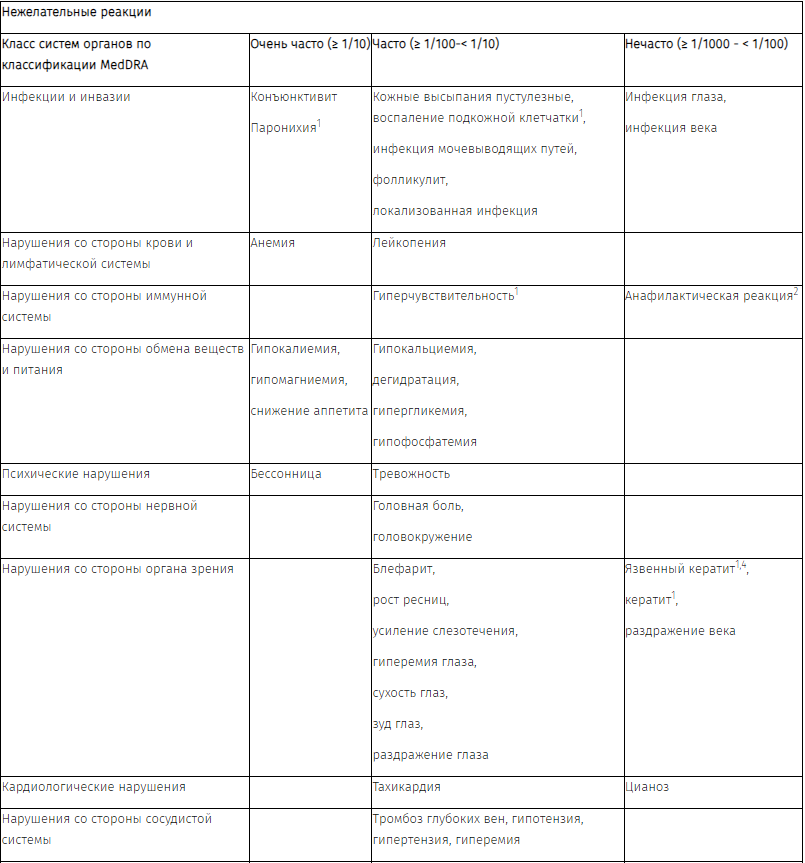
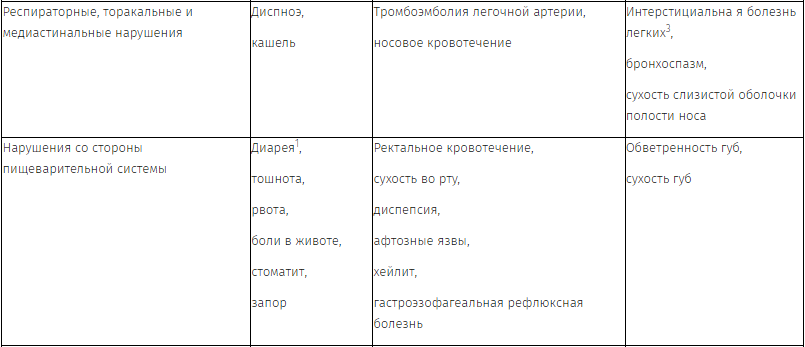
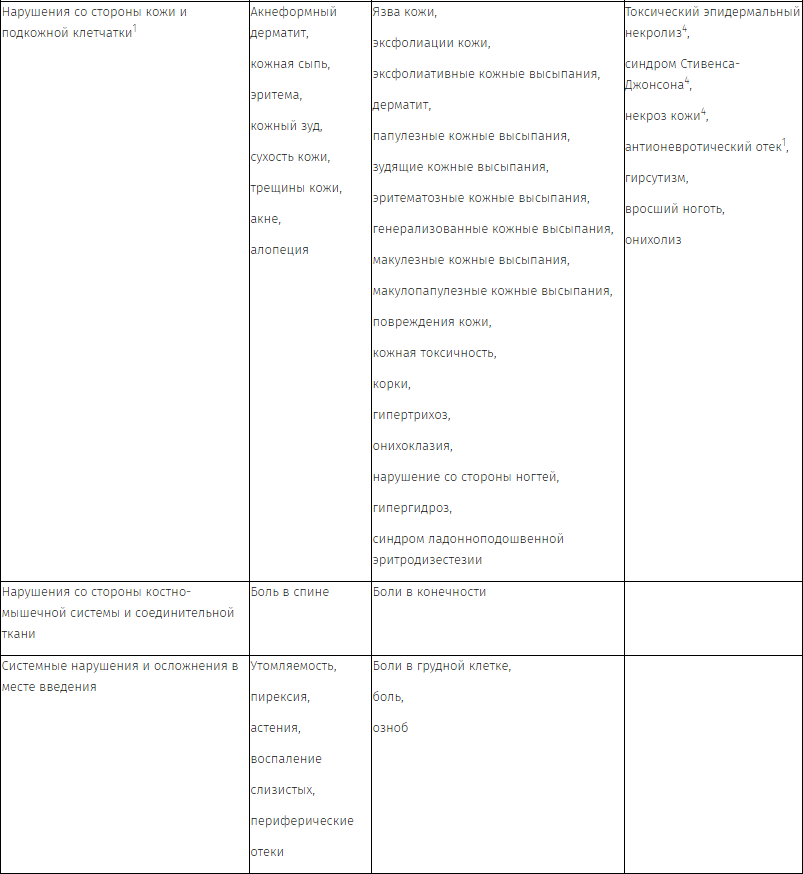
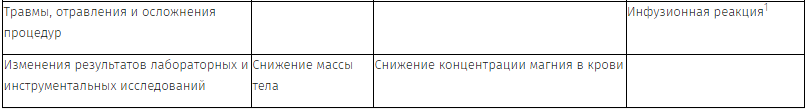
1 См. раздел «Описание отдельных нежелательных реакций».
2 См. раздел «Особые указания» (инфузионные реакции).
3 См. раздел «Особые указания» (осложнения со стороны легких).
4 Язвенный кератит, некроз кожи, синдром Стивенса-Джонсона и токсический эпидермальный некролиз являются нежелательными реакциями панитумумаба, отмечавшимися в процессе его применения после регистрации. Максимальная частота этих нежелательных реакций оценивалась на основе верхней границы 95 % доверительного интервала для точечной оценки с учетом рекомендаций регуляторных органов для оценки частоты нежелательных реакций в спонтанных сообщениях. Максимальное значение частоты, рассчитанное на основе верхней границы 95 % доверительного интервала для точечной оценки, составило 3/2244 (0,13 %).
Профиль безопасности препарата Вектибикс в комбинации с химиотерапией согласуется с зарегистрированными нежелательными реакциями препарата Вектибикс (используемого в монотерапии) и проявлениями фоновой токсичности химиотерапии. Новых проявлений токсичности или усугубления ранее известных проявлений токсичности помимо ожидаемых аддитивных эффектов не наблюдалось. Кожные реакции соответствовали наиболее часто отмечавшимся нежелательным реакциям у пациентов, получавших панитумумаб, в комбинации с химиотерапией. Другими проявлениями токсичности, отмечавшимися с большей частотой по сравнению с использованием препарата в монотерапии, являлись гипомагниемия, диарея и стоматит. Эти проявления токсичности нечасто приводили к досрочному завершению терапии препаратом Вектибикс или химиотерапии.
Описание отдельных нежелательных реакций
Нарушения со стороны пищеварительной системы
В большинстве случаев диарея имела легкую или умеренную степень тяжести. Сообщалось о тяжелых случаях диареи (степень 3 и 4 по NCI-CTC) у 2% пациентов, принимавших препарат Вектибикс в качестве монотерапии, и у 16% пациентов, принимавших препарат Вектибикс в комбинации с химиотерапией.
Сообщалось о развитии острой почечной недостаточности на фоне диареи тяжелой степени и обезвоживания (см. раздел «Особые указания»).
Инфузионные реакции
Во всех клинических исследованиях моно- и комбинированной терапии мКРР (n = 2224) реакции на инфузию (развивающиеся в течение 24 ч с момента первого введения препарата), симптомами/признаками которых могли являться озноб, повышение температуры тела или диспноэ, отмечались приблизительно у 5% пациентов, получавших препарат Вектибикс, из которых 1% были тяжелыми (3 и 4 степени NCI-CTC).
Сообщалось о развитии случая летального ангионевротического отека у пациента с рецидивирующим метастатическим плоскоклеточным раком головы и шеи, леченого препаратом Вектибикс. Фатальное осложнение развилось при возобновлении терапии после предшествующего эпизода развития ангионевротического отека. Обе реакции зафиксированы спустя более 24 часов после введения препарата (см. разделы «Противопоказания» и «Особые указания»). О реакциях гиперчувствительности, развившихся более чем через 24 часа после инфузии, также сообщалось и в пост-маркетинговый период.
Данные клинического ведения реакций на инфузию приведены в разделе «Особые указания».
Нарушения со стороны кожи и подкожно жировой клетчатки
Кожная сыпь, наиболее часто локализованная на лице, верхней части грудной клетки и спине, однако в некоторых случаях распространялась и на конечности. Как следствие тяжелых дерматологических реакций отмечали также развитие инфекционных осложнений, таких как сепсис, в редких случаях с летальным исходом, воспаление подкожной клетчатки и местные абсцессы, требующие хирургического вмешательства и дренирования. Медиана времени до развития первых проявлений дерматологических реакций составила 10 дней, а медиана времени до их разрешения с момента последнего введения препарата Вектибикс - 31 день.
Паронихиальное воспаление сопровождалось припухлостью латеральных ногтевых валиков пальцев рук и ног.
Дерматологические реакции (включая воздействие на ногти), наблюдавшиеся у пациентов, получавших препарат Вектибикс или другие ингибиторы EGFR. являются известными фармакологическими эффектами данных препаратов.
Во всех клинических исследованиях кожные реакции наблюдались приблизительно у 94% пациентов, получавших препарат Вектибикс в качестве монотерапии или в комбинации с химиотерапией (п = 2224). В основном это были сыпь и угревидный дерматит почти всегда легкого или умеренного характера. О тяжелых кожных реакциях (степень 3 по NCI-CTC) сообщалось у 23% пациентов, а о жизнеугрожающих кожных реакциях (степень 4 по NCI-CTC) - у <1% пациентов. У пациентов, получавших препарат Вектибикс, регистрировались жизнеугрожающие и летальные инфекционные осложнения, включавшие некротизирующий фасциит и сепсис (см. раздел «Особые указания»).
Данные клинического ведения дерматологических реакций, включая рекомендации по изменению дозы, приведены в разделе «Особые указания».
В пострегистрационный период применения сообщалось о редких случаях развития некрозов кожи, синдрома Стивенса-Джонсона и токсического эпидермального некролиза (см. раздел «Особые указания»).
Офтальмологическая токсичность
Сообщалось о серьезных случаях кератитов и язвенных кератитов, которые могут приводить к перфорации роговицы (см. раздел «Особые указания»).
Другие особые популяции
Не наблюдалось различий в безопасности и эффективности у пациентов пожилого возраста (≥ 65 лет), получавших монотерапию препаратом Вектибикс. Однако было зарегистрировано увеличение числа серьезных нежелательных реакций у пожилых пациентов, получавших терапию препаратом Вектибикс в комбинации с режимами химиотерапии FOLFIRI (45% по сравнению с 32%) или FOLFOX (52% по сравнению с 37%), по сравнению с получавшими только химиотерапию (см. раздел «Особые указания»). Наиболее частыми серьезными нежелательными явлениями были диарея у пациентов, получавших препарат Вектибикс в комбинации с режимами FOLFOX или FOLFIRI, дегидратация и тромбоэмболия легочной артерии - у пациентов, получавших препарат Вектибикс в комбинации с режимом FOLFIRI.
Нет данных, касающихся безопасности применения препарата Вектибикс пациентами с почечной и печеночной недостаточностью.
Достоверные данные о применении препарата Вектибикс у беременных отсутствуют. В исследованиях на животных была продемонстрирована репродуктивная токсичность препарата. Потенциальный риск ее у человека не известен. Рецептор EGF участвует в контроле пренатального развития плода и играет определенную роль в процессах нормального органогенеза, пролиферации и дифференцировки клеток развивающегося эмбриона. Таким образом, препарат Вектибикс может оказывать потенциальный вред для плода при применении у беременных женщин.
Известно, что человеческие антитела IgG способны проникать через плацентарный барьер, поэтому панитумумаб может проникать из организма матери в развивающийся организм плода. Поэтому женщины с сохранной репродуктивной функцией во время лечения препаратом Вектибикс и в течение 2 месяцев после его окончания должны использовать адекватные меры контрацепции. Если препарат Вектибикс используется в процессе беременности, или беременность развилась на фоне терапии, необходимо разъяснить пациентке потенциальный риск прерывания беременности и потенциальный вред для плода.
Грудное вскармливание
Неизвестно, проникает ли панитумумаб в грудное молоко. Так как человеческие антитела IgG проникают в грудное молоко, можно предположить, что панитумумаб может также проникать в грудное молоко. Возможность всасывания препарата и его потенциальный вред для ребенка не установлены. В период лечения препаратом Вектибикс и в течение 2 месяцев после его окончания кормление грудью не рекомендуется.
Вектибикс не должен назначаться в комбинации с режимом химиотерапии IFL или режимами химиотерапии, включающими бевацизумаб. При назначении панитумумаба в комбинации с IFL, наблюдалась высокая частота возникновения диареи тяжелой степени (см. раздел «Особые указания») и увеличивалась частота токсичности и летальных исходов при назначении панитумумаба в комбинации с режимом химиотерапии, включавшей бевацизумаб (см. раздел «Особые указания»).
Комбинация препарата Вектибикс с химиотерапией на основе оксалиплатина противопоказана пациентам с мКРР и мутациями RAS, а также пациентам с мКРР с неизвестным статусом RAS. В клиническом исследовании у пациентов с мутациями RAS в опухоли, которые получали панитумумаб и химиотерапию FOLFOX, отмечалось укорочение выживаемости без прогрессирования заболевания и общей выживаемости (см. раздел «Особые указания»).
Фармацевтическая несовместимость
Данный препарат не следует применять с другими лекарственными средствами, кроме указанных в разделе «Особые меры предосторожности при применении и утилизации».
В клинических исследованиях препарат использовался в дозах до 9 мг/кг. Были зарегистрированы случаи превышения рекомендованной терапевтической дозы (12 мг/кг) приблизительно в 2 раза. Наблюдались нежелательные эффекты, такие как токсические реакции со стороны кожи, диарея, дегидратация и повышенная утомляемость, что соответствовало профилю безопасности препарата в рекомендованной дозе.
Вектибикс может оказывать влияние на способность управлять транспортными средствами и на работу с механизмами. В случае развития нежелательных реакций со стороны органов зрения и/или снижения способности к концентрации внимания и быстроты реакции, пациентам рекомендуется воздержаться от управления транспортными средствами или работы со сложным оборудованием до разрешения указанных нежелательных реакций препарата.
- Государственный реестр лекарственных средств
- Анатомо-терапевтическо-химическая классификация (ATX)
- Международная классификация болезней (МКБ-10)
- Официальная инструкция от производителя





